- 电话:+1 2027805918 传真:+1 208640718 邮箱:info@seedoctorsinusa.com 国内电话:400-7800-120
- Copyright © 2014 - 2017 Z&L International Medical(Z&L) All Rights Reserved.
- SeeDoctorsInUSA 美国好大夫(美国好医生)operated by Z&L International Medical, LLC | Technical Support by Jing
肠癌新药
【最新消息】Ramucirumab (商品名Cyramza)用于一线治疗失败的转移性结直肠癌
2015年4月24日,美国食品和药物管理局(FDA)批准了Ramucirumab(商品名Cyramza, 美国礼来公司生产)联合FOLFIRI化疗方案,用于含贝伐单抗、奥沙利铂和氟脲嘧啶为一线治疗后疾病进展的转移性结直肠癌。Ramucirumab是一 种单克隆抗体药物,通过结和血管内皮生长因子(简称为VEGF)受体,阻止其激活而达到控制肿瘤的血管供应。
这个批准是基于一项临床试验的有效结果,正在接受含贝伐单抗、奥沙利铂和氟脲嘧啶为基础联合治疗或停止该方案治疗6 个月之内,疾病进展的结直肠癌患者,被随机分配到FOLFIRI加安慰剂组或FOLFIRI加Ramucirumab组。主要疗效终点是总生存期 (OS)。结果显示,接受FOLFIRI加Ramucirumab组的患者相对于FOLFIRI加安慰剂组的OS具有统计学意义的改善。FOLFIRI加 Ramucirumab组和FOLFIRI加安慰剂组的中位OS分别为13.3和11.7个月。Ramucirumab联合FOLFIRI组的肿瘤无恶化 生存期(PFS)也得到了显著改善,两组的中位PFS分别为5.7和4.5个月。
总体而言,安全性数据与之前已经批准的适应症的安全性数据一致。但是,基于甲状腺功能的监测,有2.6%的患者发生甲状腺功能减退。
Ramucirumab联合FOLFIRI方案的推荐剂量和用法是:8毫克/公斤体重,每2周一次,60分钟静脉输液。 Ramucirumab治疗一直持续到疾病进展或不可接受的毒性。
若需完整的处方信息,请访问:125477s011lbl
大肠癌新药: 继续使用 Bevacizumab (贝伐单抗,商品名 Avastin 阿瓦斯汀)对转移性结直肠癌有效。
2013年 1月23日,美国食品和药物管理局(FDA)批准了Bevacizumab(商品名 Avastin ?,美国基因技术公司生产),用于继续治疗在使用第一线含Bevacizumab化疗药物后病情有恶化的转移性结直肠癌(mCRC )患者。Bevacizumab将与Fluoropyrimidine-Irinotecan 或 Fluoropyrimidine-Oxaliplatin类化疗药物配合使用。
Bevacizumab是一种重组人源化单克隆IgG1 抗体,它可以结合人血管内皮生长因子(VEGF),从而阻止血管内皮生长因子与其受体的相互作用。
Bevacizumab的批准是基于最新的一个由多个国际性医疗中心共同参与的随机临床试验的有效结果。参与试验的患者都是在使用第一线 Bevacizumab-Fluoropyrimidine-Irinotecan或Bevacizumab-Fluoropyrimidine- Oxaliplatin药物治疗期间或治疗后3个月内病情恶化的转移性结直肠癌(mCRC )病人。
共有820例患者参与了该临床试验。他们被随机分配到两组治疗方案。一组接受单纯的“交叉”化疗(共411 例患者),另一组接受“交叉”化疗加Bevacizumab(共409例患者 ) 。“交叉”化疗的设计是这样的:如果患者之前接受了Fluoropyrimidine-Irinotecan为基础的化疗,新的治疗药物就用 Fluoropyrimidine-Oxaliplatin,反之亦然。第二组的唯一差别就是在“交叉”化疗的基础上再加上Bevacizumab。两组 患者的化疗都是每2或3周作一次。Bevacizumab的用药剂量为每两个星期静脉点滴5毫克/公斤或每三个星期静脉点滴7.5毫克/公斤。 Bevacizumab持续使用直至癌症明显恶化或病人不再耐受。试验结果表明,用“交叉”化疗加Bevacizumab治疗的患者比单纯用“交叉”化疗 治疗的患者总生存期(OS)有显着的改善,平均分别为11.2个月和9.8个月。接受“交叉”化疗加Bevacizumab的患者在癌症无恶化生存期 (PFS)上也比单纯接受“交叉”化疗的患者有显着的改善,平均分别为5.7个月和4.0个月。
关于Bevacizumab的全面处方信息(Prescribing information),请参阅:125085s263lbl
肠癌新药:Regorafenib(商品名Stivarga)被批准用于治疗转移性结直肠癌。
2012年9月27日,美国食品和药物管理局(FDA)批准了Regorafenib(商品名Stivarga, 德国拜耳医药保健公司生产)用于治疗转移性结直肠癌(mCRC)。患者先前已经经过Fluoropyrimidine(氟尿嘧 啶),Oxaliplatin(奥沙利铂),Irinotecan(伊立替康)为基础的化疗,抗VEGF治疗,或对KRAS野生型转移性结直肠癌的抗 EGFR治疗。
该批准是基于一项由多个国际医疗中心参与的III期临床试验的结果。共760例转移性结直肠癌患者参于该试验。所有患者之前都接受过以氟尿嘧啶,奥沙利铂 和伊立替康为基础的化疗和Bevacizumab(贝伐单抗)的治疗。除了一例KRAS野生型肿瘤患者外,其他KRAS野生型肿瘤患者都接受过 Panitumumab(帕尼单抗)或Cetuximab(西妥昔单抗)的治疗。结果显示,服用Regorafenib的患者的平均总生存期(OS)为 6.4个月,优于服用安慰剂的5.0个月。服用Regorafenib的患者的无恶化生存期(PFS)为2.0个月,也优于服用安慰剂的1.7个月。
Regorafenib最常见的不良反应(发生率大于或等于30%)包括疲劳,食欲下降,手足皮肤反应,腹泻,黏膜炎,体重减轻,感染,高血压和发音困难。最严重的不良反应有肝毒性,出血和胃肠道穿孔。
Regorafenib推荐剂量和日程为160毫克( 4个40毫克片剂),口服,每日一次,共21天,每28天为一周期。
Regorafenib(Stivarga)40毫克120片在美国的价格大约是15000美元。
若需完整的处方信息,请查看:203085lbl
大肠癌新药:Ziv-aflibercept (商品名:ZALTRAP) 对转移性结直肠癌有效。
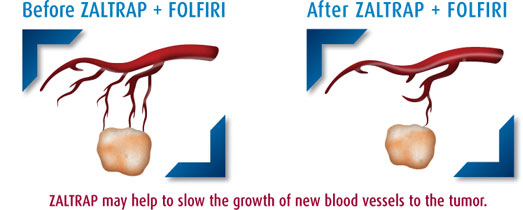
2012年8月3日,美国食品和药物管理局(FDA)批准了Ziv-aflibercept (商品名 ZALTRAP ,美国赛诺菲公司生产) 结合5 - 氟尿嘧啶,亚叶酸钙,伊立替康( FOLFIRI)联合使用,用于治疗对含奥沙利铂治疗方案无效的转移性结直肠癌。Zivaflibercept(以前被称为Aflibercept)是由 血管内皮生长因子(VEGF)受体的VEGF结合部位与IgG1免疫球蛋白的Fc部分融合的重组蛋白。
这个批准是基于一项随机的, 多个国际医疗中心参与的临床试验。患者均为转移性结直肠癌, 且在接受奥沙利铂为主的联合化疗的6个月内病情恶化。病人无论之前有无接受过贝伐单抗的治疗均可参与。
此试验共累计招收1226例患者。患者被随机分配到两组。第一组患者接受Ziv-aflibercept(剂量为4毫克/千克体重,静脉滴注,滴注时间需 超过1小时),之后加FOLFIRI (伊立替康180毫克/平方米体表面积,静脉滴注90分钟,亚叶酸钙400毫克/平方米体表面积, 静脉滴注2小时,之后再加5 - FU 400毫克/平方米体表面积, 静脉推注,最后是5 - FU 2400毫克/平方米体表面积, 持续静脉滴注 46小时)。第二组患者仅是用安慰剂代替Ziv-aflibercept ,其它药品均一样。两组的治疗周期都是每2周重复。患者接受治疗直至疾病恶化或不可耐受。主要疗效评估标准是总生存期( OS )。接受Ziv-aflibercept 治疗的患者平均总生存期为13.5个月, 而接受安慰剂治疗的患者平均总生存期则为12.06个月。Ziv-aflibercept组和安慰剂组的患者平均无恶化生存期分别为6.9个月和4.7个 月。
Ziv-aflibercept加FOLFIRI组患者最常见的副作用(见于20%以上的患者且与安慰剂组的差异达到或超过2%)为中性粒细胞减少,白细 胞减少,腹泻,蛋白尿, AST和ALT升高 ,口腔炎,乏力,血小板减少,高血压,体重下降,食欲减退,鼻出血,腹痛,发声困难,血清肌酐上升,头痛等症状。最常见的3-4级副作用(见于5%以上的 患者且与安慰剂组的差异达到或超过2%)为中性粒细胞减少,腹泻,高血压,白细胞减少,口腔炎,乏力,蛋白尿。
Ziv-aflibercept有可能导致严重的,有时甚至是致命的出血,包括胃肠道出血。接受Ziv-aflibercept加FOLFIRI的患者有 2.9 %出现 3-4级出血事件, 而接受安慰剂加FOLFIRI的患者则为1.7%。除了出血,Ziv-aflibercept的黑框警告还注明胃肠道穿孔和伤口不能愈合的风险。
接受Ziv-aflibercept加FOLFIRI的患者有2.6 %出现动脉血栓, 而接受安慰剂加FOLFIRI的患者则为1.7%。Ziv-aflibercept也可能增加静脉血栓的机会。接受Ziv-aflibercept加 FOLFIRI的患者有9%出现静脉血栓, 而接受安慰剂加FOLFIRI的患者则为7%。Ziv-aflibercept还可能增加瘘管形成和可逆性后部白质脑病综合征的机会 。
Ziv-aflibercept的推荐剂量和时间为4毫克/千克体重,静脉滴注,滴注时间需超过1小时,每2周一次,与FOLFIRI治疗方案同时使用。
若需完整的处方信息, 请查阅:125418s000lbl
2015年4月24日,美国食品和药物管理局(FDA)批准了Ramucirumab(商品名Cyramza, 美国礼来公司生产)联合FOLFIRI化疗方案,用于含贝伐单抗、奥沙利铂和氟脲嘧啶为一线治疗后疾病进展的转移性结直肠癌。Ramucirumab是一 种单克隆抗体药物,通过结和血管内皮生长因子(简称为VEGF)受体,阻止其激活而达到控制肿瘤的血管供应。
这个批准是基于一项临床试验的有效结果,正在接受含贝伐单抗、奥沙利铂和氟脲嘧啶为基础联合治疗或停止该方案治疗6 个月之内,疾病进展的结直肠癌患者,被随机分配到FOLFIRI加安慰剂组或FOLFIRI加Ramucirumab组。主要疗效终点是总生存期 (OS)。结果显示,接受FOLFIRI加Ramucirumab组的患者相对于FOLFIRI加安慰剂组的OS具有统计学意义的改善。FOLFIRI加 Ramucirumab组和FOLFIRI加安慰剂组的中位OS分别为13.3和11.7个月。Ramucirumab联合FOLFIRI组的肿瘤无恶化 生存期(PFS)也得到了显著改善,两组的中位PFS分别为5.7和4.5个月。
总体而言,安全性数据与之前已经批准的适应症的安全性数据一致。但是,基于甲状腺功能的监测,有2.6%的患者发生甲状腺功能减退。
Ramucirumab联合FOLFIRI方案的推荐剂量和用法是:8毫克/公斤体重,每2周一次,60分钟静脉输液。 Ramucirumab治疗一直持续到疾病进展或不可接受的毒性。
若需完整的处方信息,请访问:125477s011lbl

大肠癌新药: 继续使用 Bevacizumab (贝伐单抗,商品名 Avastin 阿瓦斯汀)对转移性结直肠癌有效。
2013年 1月23日,美国食品和药物管理局(FDA)批准了Bevacizumab(商品名 Avastin ?,美国基因技术公司生产),用于继续治疗在使用第一线含Bevacizumab化疗药物后病情有恶化的转移性结直肠癌(mCRC )患者。Bevacizumab将与Fluoropyrimidine-Irinotecan 或 Fluoropyrimidine-Oxaliplatin类化疗药物配合使用。
Bevacizumab是一种重组人源化单克隆IgG1 抗体,它可以结合人血管内皮生长因子(VEGF),从而阻止血管内皮生长因子与其受体的相互作用。
Bevacizumab的批准是基于最新的一个由多个国际性医疗中心共同参与的随机临床试验的有效结果。参与试验的患者都是在使用第一线 Bevacizumab-Fluoropyrimidine-Irinotecan或Bevacizumab-Fluoropyrimidine- Oxaliplatin药物治疗期间或治疗后3个月内病情恶化的转移性结直肠癌(mCRC )病人。
共有820例患者参与了该临床试验。他们被随机分配到两组治疗方案。一组接受单纯的“交叉”化疗(共411 例患者),另一组接受“交叉”化疗加Bevacizumab(共409例患者 ) 。“交叉”化疗的设计是这样的:如果患者之前接受了Fluoropyrimidine-Irinotecan为基础的化疗,新的治疗药物就用 Fluoropyrimidine-Oxaliplatin,反之亦然。第二组的唯一差别就是在“交叉”化疗的基础上再加上Bevacizumab。两组 患者的化疗都是每2或3周作一次。Bevacizumab的用药剂量为每两个星期静脉点滴5毫克/公斤或每三个星期静脉点滴7.5毫克/公斤。 Bevacizumab持续使用直至癌症明显恶化或病人不再耐受。试验结果表明,用“交叉”化疗加Bevacizumab治疗的患者比单纯用“交叉”化疗 治疗的患者总生存期(OS)有显着的改善,平均分别为11.2个月和9.8个月。接受“交叉”化疗加Bevacizumab的患者在癌症无恶化生存期 (PFS)上也比单纯接受“交叉”化疗的患者有显着的改善,平均分别为5.7个月和4.0个月。
关于Bevacizumab的全面处方信息(Prescribing information),请参阅:125085s263lbl

肠癌新药:Regorafenib(商品名Stivarga)被批准用于治疗转移性结直肠癌。
2012年9月27日,美国食品和药物管理局(FDA)批准了Regorafenib(商品名Stivarga, 德国拜耳医药保健公司生产)用于治疗转移性结直肠癌(mCRC)。患者先前已经经过Fluoropyrimidine(氟尿嘧 啶),Oxaliplatin(奥沙利铂),Irinotecan(伊立替康)为基础的化疗,抗VEGF治疗,或对KRAS野生型转移性结直肠癌的抗 EGFR治疗。
该批准是基于一项由多个国际医疗中心参与的III期临床试验的结果。共760例转移性结直肠癌患者参于该试验。所有患者之前都接受过以氟尿嘧啶,奥沙利铂 和伊立替康为基础的化疗和Bevacizumab(贝伐单抗)的治疗。除了一例KRAS野生型肿瘤患者外,其他KRAS野生型肿瘤患者都接受过 Panitumumab(帕尼单抗)或Cetuximab(西妥昔单抗)的治疗。结果显示,服用Regorafenib的患者的平均总生存期(OS)为 6.4个月,优于服用安慰剂的5.0个月。服用Regorafenib的患者的无恶化生存期(PFS)为2.0个月,也优于服用安慰剂的1.7个月。
Regorafenib最常见的不良反应(发生率大于或等于30%)包括疲劳,食欲下降,手足皮肤反应,腹泻,黏膜炎,体重减轻,感染,高血压和发音困难。最严重的不良反应有肝毒性,出血和胃肠道穿孔。
Regorafenib推荐剂量和日程为160毫克( 4个40毫克片剂),口服,每日一次,共21天,每28天为一周期。
Regorafenib(Stivarga)40毫克120片在美国的价格大约是15000美元。
若需完整的处方信息,请查看:203085lbl
大肠癌新药:Ziv-aflibercept (商品名:ZALTRAP) 对转移性结直肠癌有效。
2012年8月3日,美国食品和药物管理局(FDA)批准了Ziv-aflibercept (商品名 ZALTRAP ,美国赛诺菲公司生产) 结合5 - 氟尿嘧啶,亚叶酸钙,伊立替康( FOLFIRI)联合使用,用于治疗对含奥沙利铂治疗方案无效的转移性结直肠癌。Zivaflibercept(以前被称为Aflibercept)是由 血管内皮生长因子(VEGF)受体的VEGF结合部位与IgG1免疫球蛋白的Fc部分融合的重组蛋白。
这个批准是基于一项随机的, 多个国际医疗中心参与的临床试验。患者均为转移性结直肠癌, 且在接受奥沙利铂为主的联合化疗的6个月内病情恶化。病人无论之前有无接受过贝伐单抗的治疗均可参与。
此试验共累计招收1226例患者。患者被随机分配到两组。第一组患者接受Ziv-aflibercept(剂量为4毫克/千克体重,静脉滴注,滴注时间需 超过1小时),之后加FOLFIRI (伊立替康180毫克/平方米体表面积,静脉滴注90分钟,亚叶酸钙400毫克/平方米体表面积, 静脉滴注2小时,之后再加5 - FU 400毫克/平方米体表面积, 静脉推注,最后是5 - FU 2400毫克/平方米体表面积, 持续静脉滴注 46小时)。第二组患者仅是用安慰剂代替Ziv-aflibercept ,其它药品均一样。两组的治疗周期都是每2周重复。患者接受治疗直至疾病恶化或不可耐受。主要疗效评估标准是总生存期( OS )。接受Ziv-aflibercept 治疗的患者平均总生存期为13.5个月, 而接受安慰剂治疗的患者平均总生存期则为12.06个月。Ziv-aflibercept组和安慰剂组的患者平均无恶化生存期分别为6.9个月和4.7个 月。
Ziv-aflibercept加FOLFIRI组患者最常见的副作用(见于20%以上的患者且与安慰剂组的差异达到或超过2%)为中性粒细胞减少,白细 胞减少,腹泻,蛋白尿, AST和ALT升高 ,口腔炎,乏力,血小板减少,高血压,体重下降,食欲减退,鼻出血,腹痛,发声困难,血清肌酐上升,头痛等症状。最常见的3-4级副作用(见于5%以上的 患者且与安慰剂组的差异达到或超过2%)为中性粒细胞减少,腹泻,高血压,白细胞减少,口腔炎,乏力,蛋白尿。
Ziv-aflibercept有可能导致严重的,有时甚至是致命的出血,包括胃肠道出血。接受Ziv-aflibercept加FOLFIRI的患者有 2.9 %出现 3-4级出血事件, 而接受安慰剂加FOLFIRI的患者则为1.7%。除了出血,Ziv-aflibercept的黑框警告还注明胃肠道穿孔和伤口不能愈合的风险。
接受Ziv-aflibercept加FOLFIRI的患者有2.6 %出现动脉血栓, 而接受安慰剂加FOLFIRI的患者则为1.7%。Ziv-aflibercept也可能增加静脉血栓的机会。接受Ziv-aflibercept加 FOLFIRI的患者有9%出现静脉血栓, 而接受安慰剂加FOLFIRI的患者则为7%。Ziv-aflibercept还可能增加瘘管形成和可逆性后部白质脑病综合征的机会 。
Ziv-aflibercept的推荐剂量和时间为4毫克/千克体重,静脉滴注,滴注时间需超过1小时,每2周一次,与FOLFIRI治疗方案同时使用。
若需完整的处方信息, 请查阅:125418s000lbl


