- 电话:+1 2027805918 传真:+1 208640718 邮箱:info@seedoctorsinusa.com 国内电话:400-7800-120
- Copyright © 2014 - 2017 Z&L International Medical(Z&L) All Rights Reserved.
- SeeDoctorsInUSA 美国好大夫(美国好医生)operated by Z&L International Medical, LLC | Technical Support by Jing
荧光下看到的的癌细胞先期转移模式 Nature 531
Visualization of immediate immune responses to pioneer metastatic cells in the lung
-
Nature - 531,
- 513–517
- doi:10.1038/nature16985
- Received
- Accepted
- Published online
Lung metastasis is the lethal determinant in many cancers1, 2 and a number of lines of evidence point to monocytes and macrophages having key roles in its development3, 4, 5. Yet little is known about the immediate fate of incoming tumour cells as they colonize this tissue, and even less known about how they make first contact with the immune system. Primary tumours liberate circulating tumour cells (CTCs) into the blood and we have developed a stable intravital two-photon lung imaging model in mice6 for direct observation of the arrival of CTCs and subsequent host interaction. Here we show dynamic generation of tumour microparticles in shear flow in the capillaries within minutes of CTC entry. Rather than dispersing under flow, many of these microparticles remain attached to the lung vasculature or independently migrate along the inner walls of vessels. Using fluorescent lineage reporters and flow cytometry, we observed ‘waves’ of distinct myeloid cell subsets that load differentially and sequentially with this CTC-derived material. Many of these tumour-ingesting myeloid cells collectively accumulated in the lung interstitium along with the successful metastatic cells and, as previously understood, promote the development of successful metastases from surviving tumour cells3. Although the numbers of these cells rise globally in the lung with metastatic exposure and ingesting myeloid cells undergo phenotypic changes associated with microparticle ingestion, a consistently sparse population of resident conventional dendritic cells, among the last cells to interact with CTCs, confer anti-metastatic protection. This work reveals that CTC fragmentation generates immune-interacting intermediates, and defines a competitive relationship between phagocyte populations for tumour loading during metastatic cell seeding.
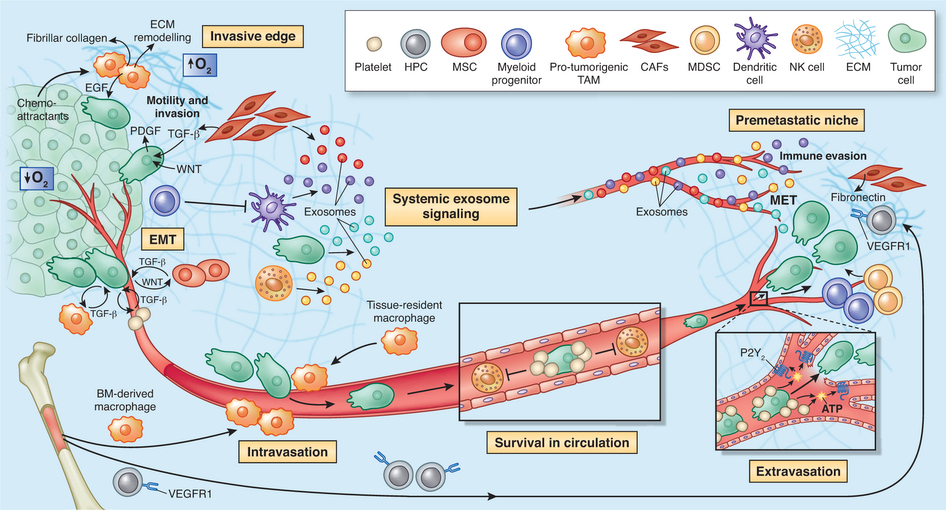
美国加州大学旧金山分校的研究人员首次能够在转移癌模式小鼠体内直接观察当浸润性癌细胞向肺部迁移时发现:早期的“先锋”癌细胞进入肺部后通常都会死亡,但是它们首先释放出类似于僵尸的颗粒,这些颗粒能够自行移动,并且被一波又一波的免疫细胞吞噬。在这些免疫细胞中,很多细胞只要被这些癌症颗粒感染,就会进入肺部组织深处,从而为在血液中漂浮的癌细胞未来能够安全地安营扎寨和形成新的转移灶开辟道路。相关研究结果于2016年3月16日在线发表在Nature期刊上。
论文通信作者、加州大学旧金山分校病理学教授Matthew "Max" Krummel博士说,“我们之前总是认为进入健康组织的浸润性癌细胞要么存活袭来产生转移性肿瘤,要么死掉而前功尽弃。令我们吃惊的是,我们观察到当癌细胞碎裂和死亡时,它们将免疫细胞变成它们的搭档,从而为癌细胞下次到来铺平道路。”
Krummel和他的研究团队认为对先锋癌细胞和免疫系统在早期如何相互作用以及免疫系统如何为转移癌作好铺垫的这种全新理解将导致人们开发出更好的方法来治疗和预防人体内的浸润性癌症。 在诸如肺部、大脑和肝脏之类的至关重要器官中的浸润性转移瘤(invasive metastases)是绝大多数癌症死亡的原因,但是在此之前,人们对这种肿瘤转移过程本身知之甚少。已知癌细胞让免疫细胞提供合作,将靶组织软化以便转移性肿瘤浸润,但是人们一直以来并不知道身体中的保护性免疫细胞如何变成叛徒。一种主导理论提示着肿瘤产生分子信号,对免疫系统进行重编程,从而让新的癌症转移灶扎根,但是这些信号实际上如何与靶组织中的免疫反应相互作用仍是个未知数。很少有研究人员能够直接观察转移性浸润的第一阶段,因而也就不能理解为何一些新的癌症转移灶茁壮成长,而另一些消退。但是近几年,来自Krummel实验室的研究人员利用一种双光子显微技术完美地实现在癌细胞到达小鼠肺部首个24小时期间稳定地对这些癌细胞进行成像。Krummel解释道,这是个卓越的成就,这是因为肺部在每次呼吸时前后移动几毫米,这就使得科学家们通常不可能观察到尺寸只有这种移动距离千分之一的微小癌细胞。
论文第一作者、加州大学旧金山分校博士后研究员Mark B. Headley博士说,“在开始这项研究之前,它就像似循环肿瘤细胞进入暗盒,然后当转移瘤基本上产生时出现。我们如今在很大程度上为这些转移性肿瘤产生的早期阶段打开一扇窗。” 来自Krummel实验室的Headley及其同事们将黑色素瘤细胞注射进小鼠血液中,并追踪这些癌细胞到达肺部,在那里,他们观察到一种他们从未曾想象到的奇怪和恐怖的场面。早些的侵入性免疫细胞被血液流动的力量吹打成碎片,但是它们碎裂的残骸也有它们自己的生命。研究人员随后还观察到对喧哗保持警惕的免疫细胞围住这些癌症碎片,并吞噬它们。但是这首批细胞应答器(即免疫细胞)的行为很快开始变得非常怪异:它们离开毛细血管,而且似乎为肺部组织本身未来的癌细胞到达构建出保护性巢穴。
Krummel和同事们发现并不是所有免疫细胞都会受到癌症颗粒的欺骗。在将癌细胞注射到小鼠体内之后,研究人员观察到几波不同的免疫细胞到达肺部。很多早期作出反应的免疫细胞---如单核细胞和巨噬细胞---继续帮助后来的癌细胞在肺部站住脚跟。另一方面,树突细胞通常较晚地到达现场,但是似乎将癌症视作威胁:在吞噬癌细胞颗粒后,它们迁移到小鼠淋巴结,激活其他的免疫细胞,这些免疫细胞激活后,能够返回肺部并且攻击任何刚出现的转移灶。
Krummel说,这种认识针对为何一些浸润性癌症能够站位脚跟而另一些不能,提出一种新的假设。“在成功的肿瘤转移中,我们认为存在不平衡,即太多免疫细胞经肿瘤重编程后将癌细胞视为无害的,太少的免疫细胞获得这些癌细胞是危险的或不同的信息。” 他说,这种猜测有可能为有风险患上转移性癌症的病人开发新的治疗方法开启大门,比如,试图抑制容易受骗的免疫细胞以便阻止它们帮助新的癌细胞站位脚跟,与此同时加强更加精明的树突细胞的活性从而促进合适的免疫反应以便除去任何新的转移灶。
